-
-
-
Tổng tiền thanh toán:
-
Cách viết công thức cấu tạo của H2S04, HN03 theo quy tắc bát tử
Đăng bởi CÔNG TY CỔ PHẦN ĐẦU TƯ THƯƠNG MẠI VÀ DỊCH VỤ GIA KHÁNH
Thứ Sun,
30/05/2021
Bài viết sẽ chia sẻ với các bạn cách viết công thức cấu tạo của H2SO4, HN03 theo 2 cách: quy tắc bát tử và cách viết thông thường.
Quy tắc bát tử là gì
Quy tắc bát tử là quy tắc viết công thức electron của một chất sao cho đảm bảo số electron của mỗi nguyên tử là 8 tức đạt được cấu hình bền của khí hiếm hoặc 2 electron đối với Heli.
Quy tắc này chỉ đúng với những nguyên tố thuộc chu kì I và II
(Nội dung này được học trong chương trình SGK nâng cao lớp 10)
4 bước viết Công thức cấu tạo hợp chất vô cơ theo quy tắc bát tử
Để viết công thức cấu tạo các hợp chất vô cơ khi biết công thức phân tử của chúng, chúng ta có thể thực hiện các bước như sau:
 Bước 1: Xác định tổng số e mà các nguyên tử mà từng nguyên tố cần cho hay nhận để đạt cấu hình bền vững theo quy tắc bát tử (lớp ngoài cùng có 8 e, đối với Heli thì lớp ngoài cùng có 2e là bền vững).
Bước 1: Xác định tổng số e mà các nguyên tử mà từng nguyên tố cần cho hay nhận để đạt cấu hình bền vững theo quy tắc bát tử (lớp ngoài cùng có 8 e, đối với Heli thì lớp ngoài cùng có 2e là bền vững).
- Đối với phi kim thì tính số e nhận thêm.
- Đối với kim loại thì tính số e nhường đi.
 Bước 2: Xác định tổng số e của tất cả các nguyên tố cần để đạt cấu hình bền vững theo quy tắc bát tử (xét tổng của toàn bộ phân tử).
Bước 2: Xác định tổng số e của tất cả các nguyên tố cần để đạt cấu hình bền vững theo quy tắc bát tử (xét tổng của toàn bộ phân tử).
 Bước 3: Tính số liên kết tồn tại trong phân tử hợp chất đó. Vì mỗi liên kết cộng hóa trị là sự góp chung 2e từ hai nguyên tử → mỗi liên kết chứa 2e.
Bước 3: Tính số liên kết tồn tại trong phân tử hợp chất đó. Vì mỗi liên kết cộng hóa trị là sự góp chung 2e từ hai nguyên tử → mỗi liên kết chứa 2e.
Số liên kết = (tổng số e mà phân tử cần để đảm bảo quy tắc bát tử (tổng số e mà phân tử cần để đảm bảo quy tác bát tử): 2
 Bước 4: Sắp xếp các nguyên tử sao đúng trật tự của chúng và tổng số liên kết phải bằng tổng số liên kết để tính ở trên.
Bước 4: Sắp xếp các nguyên tử sao đúng trật tự của chúng và tổng số liên kết phải bằng tổng số liên kết để tính ở trên.
Cách viết công thức cấu tạo H2SO4 theo quy tắc bát tử
- 1 nguyên tử H cần thêm 1e để thỏa mãn quy tắc bát tử, nhị tử. Mà phân tử H2SO4 có hai nguyên tử nên cần 2e.
- 1 nguyên tử S cần 2e.
- 1 nguyên tử O cần 2e →4 nguyên tử cần 8e
- Tổng số e mà 2 nguyên tử H, 4 nguyên tử O,1 nguyên tử S cần là:
a = 2+2+ 8 = 12e
Tổng số liên kết có trong phân tử H2SO4 : N = a:2 = 6
- Vì trong phân tử axit có oxi luôn tồn tại nhóm H-O- Mà phân tử H2SO4 có 2 nguyên tử H nên có 2 nhóm HO- .
- Viết các lên kết giữa các nhóm H-O- với S trước rồi tính số liên kết còn lại là 2 viết cho 2 nguyên tử O còn lại bằng các liên kết cho nhận.
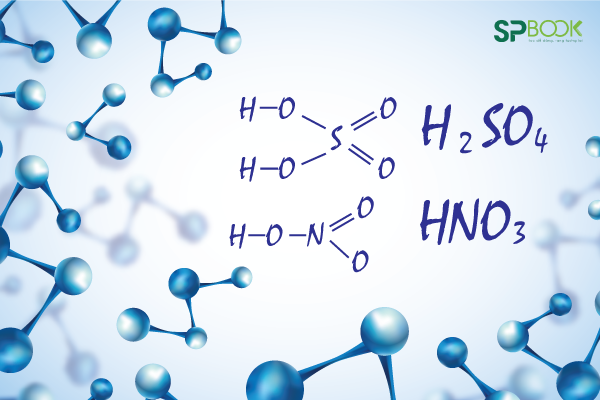
Vậy công thức cấu tạo của H2SO4 là:
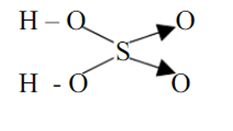
Đây là công thức viết theo quy tắc bát tử. Nếu chúng ta viết công thức như sau vẫn được chấp nhận (nhưng nó không thoả mãn quy tắc bát tử):
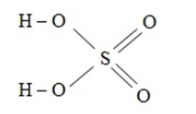
Cách viết công thức cấu tạo HNO3 theo quy tắc bát tử
-1 nguyên tử H cần nhận thêm 1 e
-1 nguyên tử N cần nhận thêm 3 e
-3 nguyên tử O cần nhận thêm 6 e
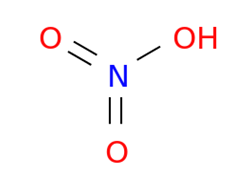
- Tổng số e mà toàn phân tử cần là 10 e. Suy ra số liên kết trong phân tử là 5 liên kết. Vậy công thức cấu tạo của HNO3 là:
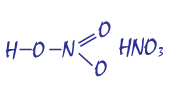
Hoặc chúng ta viết công thức như sau vẫn được chấp nhận (nhưng nó không thoả mãn quy tắc bát tử)
Chú ý:
- Phương pháp này chỉ áp dụng cho các hợp chất vô cơ có bản chất liên kết cộng hóa trị trong phân tử.
- Vì bản thân quy tắc bát tử không nghiệm đúng với tất cả các hợp chất hóa học nên phương pháp này cũng nhận các thiếu sót đó.
- Phương pháp này dựa trên nền tảng quy tắc bát tử. Nhưng áp dụng được với đa số hợp chất vô cơ nên có thể giúp các bạn giải nhanh các bài tập dạng này và xác đinh dạng lai hóa của các nguyên tử trung tâm nhanh hơn.
- Nó không nghiệm đúng với các hợp chất: NO, NO2 ……..
| Các kiến thức khác liên quan đến H2SO4 và HNO3 cũng được đề cập rõ hơn ở chương 5 cuốn sách Làm chủ môn Hóa trong 30 ngày - Tập 2 ( Hóa Vô cơ). Các em có thể tham khảo thêm về sách tại đây. |
Tin tức khác:
- Phổ điểm chi tiết tất cả các môn thi THPT quốc gia 2023 đối sánh với 2022 - phần 4 (Lịch sử, Địa lí)(18/07/2023)
- Phổ điểm chi tiết tất cả các môn thi THPT quốc gia 2023 đối sánh với 2022 - phần 3 (Hóa học, Sinh học)(18/07/2023)
- Phổ điểm chi tiết tất cả các môn thi THPT quốc gia 2023 đối sánh với 2022 - phần 2 (Tiếng Anh, Vật lí)(18/07/2023)
- Phổ điểm chi tiết tất cả các môn thi THPT quốc gia 2023 đối sánh với 2022 - phần 1 (Toán, Văn)(18/07/2023)
- Nhận định chi tiết về phổ điểm môn ngữ văn thi THPT Quốc gia 2023(18/07/2023)
- Nhận định chi tiết về phổ điểm môn toán thi THPT Quốc gia 2023(18/07/2023)
Bình luận:
86 bình luận
Jerrygep
04/12/2022кредити та гроші [url=https://pro-groshi.info/]https://pro-groshi.info/[/url]
Raymondbuilk
04/12/2022заработок в интернте [url=https://infomagaz.xyz/]https://infomagaz.xyz/[/url]
BryanEmpig
03/12/2022бізнес в інтернеті [url=https://dive-club.com.ua/]https://dive-club.com.ua/[/url]
VictorRon
03/12/2022блог о деньгах [url=https://euromoneys.com/]https://euromoneys.com/[/url]


DavidDab Trả lời
04/12/2022бізнес онлайн [url=https://sladent.com.ua/]https://sladent.com.ua/[/url]